CRISPR-Cas9 in het menselijk lichaam
Voor het eerst is een veelbelovende techniek voor het bewerken van DNA gebruikt in een patiënt. Onderzoekers en artsen in de Verenigde Staten zetten CRISPR-Cas9 in om een erfelijke oogaandoening te behandelen.
Bij een klinische studie naar de inzet van CRISPR-Cas9 in het menselijk lichaam is de eerste patiënt met CRISPR-Cas9 gentherapie behandeld. De studie is een samenwerking van een team van wetenschappers van Oregon Health & Science University in Portland (Verenigde Staten) in samenwerking met Editas Medicine in Massachusetts en het Ierse Allergan plc.
Lichtgevoelige cellen
In deze studie wordt de methode gebruikt om een vorm van de genetische oogaandoening Leber congenitale amaurosis (LCA) te behandelen. Bij deze vorm van LCA, LCA10, zijn de lichtgevoelige cellen uitgeschakeld door een genetische afwijking, wat al binnen het eerste levensjaar kan leiden tot ernstige slechtziendheid of blindheid.
Het de bedoeling dat het CRISPR-Cas9-medicijn de mutatie van het gen CEP290 verwijdert die verantwoordelijk is voor de afwijking. Het medicijn is direct in het oog geïnjecteerd, in de buurt van de lichtgevoelige cellen. Juist omdat de cellen alleen geïnactiveerd zijn door de mutatie in het DNA, hopen de wetenschappers dat reactivatie van deze cellen het zicht van de patiënt weer verbetert.
Het Nederlandse bedrijf ProQR is ook bezig de lichtgevoelige cellen te reactiveren via een andere behandeling om de erfelijke oogaandoening tegen te gaan. De voorlopige resultaten van deze studie zijn voorzichtig positief over de effecteren van de reactivatie.
Knippen
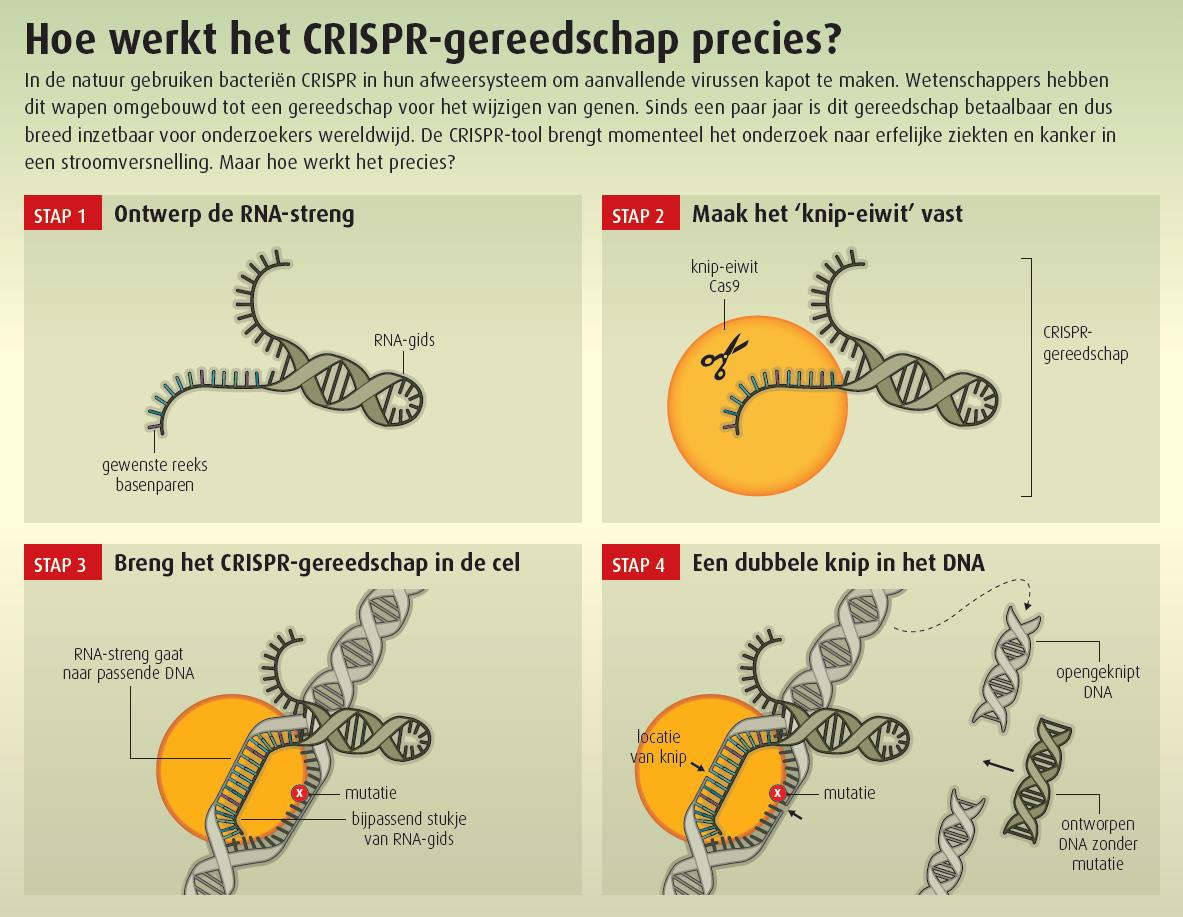
CRISPR-Cas9 is een methode voor DNA bewerking met grote precisie. Het is afgekeken van het afweersysteem van bacteriën. De truc van bacteriën kan als volgt gebruikt worden voor het bewerken van genen. Cas9 wordt met een stuk RNA als gids en een stuk DNA als vervanger de cel in gestuurd. Het stuk RNA komt overeen met het stuk DNA in de cel dat weggeknipt moet worden en dient om Cas9 op de juiste locatie te krijgen. Daarnaast krijgt Cas9 het nieuwe stuk DNA mee wat het oude deel moet vervangen. In de cel gaat het eiwit opzoek naar het stuk overeenkomend DNA om dit weg te knippen te vervangen door het nieuwe stuk DNA.
Buiten het lichaam
In eerdere proeven werden menselijke cellen buiten het lichaam behandeld om vervolgens weer in het lichaam gebracht te worden. Volgens Fyodor Urnov, onderzoeker aan University of California in Berkeley, gespecialiseerd in op CRISPR-gebaseerd DNA-bewerking, is het gebruik van CRISPR-Cas9 in het menselijk lichaam in plaats van in een petrischaaltje, een grote stap. In een nieuwsbericht van Nature zegt hij: 'Het is te vergelijken met een ruimtevlucht versus een gewone vliegreis.'
Voor dit onderzoek willen de wetenschappers in totaal achttien mensen testen. Ze plannen dit onderzoek afgerond te hebben in 2024.
Virale gentherapie
Al eerder probeerden wetenschappers gentherapie direct in het lichaam. Dit was voor het Hunter’s syndroom, een leverafwijking waarbij het lichaam van de patiënt bepaalde complexe suikers niet kan afbreken. Hierbij werd het medicijn in de lever geïnjecteerd. In deze klinische trials gebruikten de onderzoekers gentherapie met behulp van virussen. Hierbij wordt een virus gebruikt om het stuk therapeutisch DNA in de cel te krijgen.
Beeldmateriaal: depositphotos