Nobelprijs chemie voor voorspellen en namaken van eiwitstructuren
De Nobelprijs voor Scheikunde ging dit jaar naar Demis Hassabis en John Jumper van Google DeepMind en David Baker van de Universiteit van Washington. Baker bedacht in 2003 een manier om eiwitten uit losse aminozuren samen te stellen. Hassabis en Jumper ontwikkelden een AI-algoritme dat voorspelt hoe aminozuurketens zich tot driedimensionale eiwitten vouwen. Over dit laatste onderzoek schreven wij op 1 december 2020 onderstaand artikel.
Met computerkracht en kunstmatige intelligentie zijn de ingenieurs van DeepMind erin geslaagd om bijna perfect te voorspellen hoe onbekende eiwitten precies zullen vouwen. Dankzij dit rekenwerk kunnen mogelijk ziekten beter worden begrepen en daardoor gerichter medicijnen bedacht.
Tijdens een tweejaarlijkse wedstrijd voor het rekenen aan eiwitten heeft het bedrijf DeepMind (sinds 2014 onderdeel van Google) een ongeëvenaarde precisie gehaald, zo liet het bedrijf gisteren weten in een uitgebreide blogpost.
Beter dan ooit kan software berekenen hoe een eiwit zal vouwen, op basis van de reeks aminozuren waaruit het is opgebouwd. Biologen en biochemici spreken van een grote doorbraak. ‘Dit is mooi werk, maar het verrast me niet. Ik wist waarmee DeepMind bezig was, want ook in 2018 boekten ze al mooie resultaten’, zegt Alexandre Bonvin, hoogleraar Computational Structural Biology aan de Universiteit Utrecht. ‘Nu heeft het bedrijf zich verder verbeterd.’
Bonvin kraakt ook een kritische noot. ‘De resultaten van de wedstrijd zijn geweldig, daar is niets op af te dingen. Maar de DeepMind-ingenieurs hebben hun software nog niet vrijgegeven en nog geen wetenschappelijk artikel gepubliceerd. Dus collega-wetenschappers hebben nog niet kunnen zien hóe ze het precies doen.’
Platte vlak
In de wondere wereld van de scheikunde zijn maar weinig moleculen die in het platte vlak bestaan. Mini-moleculen als CO2 en H2O zijn toevallig tweedimensionaal, maar als moleculen ook maar een beetje groter worden, nemen ze een driedimensionale vorm aan. Ketens van atomen gaan dan knikken en vouwen over hoeken die worden bepaald door de interactie van de grenzen van het molecuul met zichzelf.
Machinerie
Die driedimensionale structuur heeft bovendien een functie. Neem eiwitten, de grote complexe moleculen die de machinerie van ons lichaam (en dat van veel andere organismen) aan de gang houden. Ze laten chemische reacties verlopen (als enzymen), vallen indringers aan (als antilichamen) of fungeren als chemische boodschappers (hormonen, zoals insuline). Ben je volledig gezond, dan doen de eiwitten precies wat ze moeten doen, maar veel ziekten hangen samen met problemen met eiwitten.
Op de juiste manier vouwen
Eiwitten zijn opgebouwd uit lange ketens van aminozuren (een beperkte collectie) waarbij de ordening van die elementen bepaalt hoe een specifiek eiwit vouwt. In het lichaam is niet alleen de chemische formule van een eiwit van belang, maar ook de manier waarop het zich vouwt. Sterker nog, er zijn zelfs ziekten die worden veroorzaakt door een eiwit dat niet op de juiste manier vouwt.
Dat is de belangrijkste reden dat biowetenschappers onderzoek doen naar het vouwen van eiwitten. Daarvoor hebben ze door de jaren heen verschillende technieken ontwikkeld. Ten eerste kunnen ze bestaande eiwitten ‘bekijken’ in het laboratorium met technieken zoals röntgenkristallografie en NMR-spectroscopie. Met de beelden die dit oplevert kunnen wetenschappers uitpuzzelen welke driedimensionale vorm ontstaat als een lange reeks aminozuren aan elkaar is geplakt.
Voorspellen
Maar de heilige graal in dit vakgebied is om vooraf te kunnen voorspellen hoe een nieuwe lange keten van aminozuren zal vouwen. Om het onderzoek hiernaar een duwtje in de rug te geven hebben wetenschappers de tweejaarlijkse wedstrijd CASP (Community Wide Experiment on the Critical Assessment of Techniques for Protein Structure Prediction) in het leven geroepen. Wanneer die plaatsvindt, gaan zo’n honderd teams uit twintig landen aan de slag met computers en software om te voorspellen hoe een nieuw verzonnen eiwit er in drie dimensies zal uitzien. Gisteren ging de editie van 2020 van start.
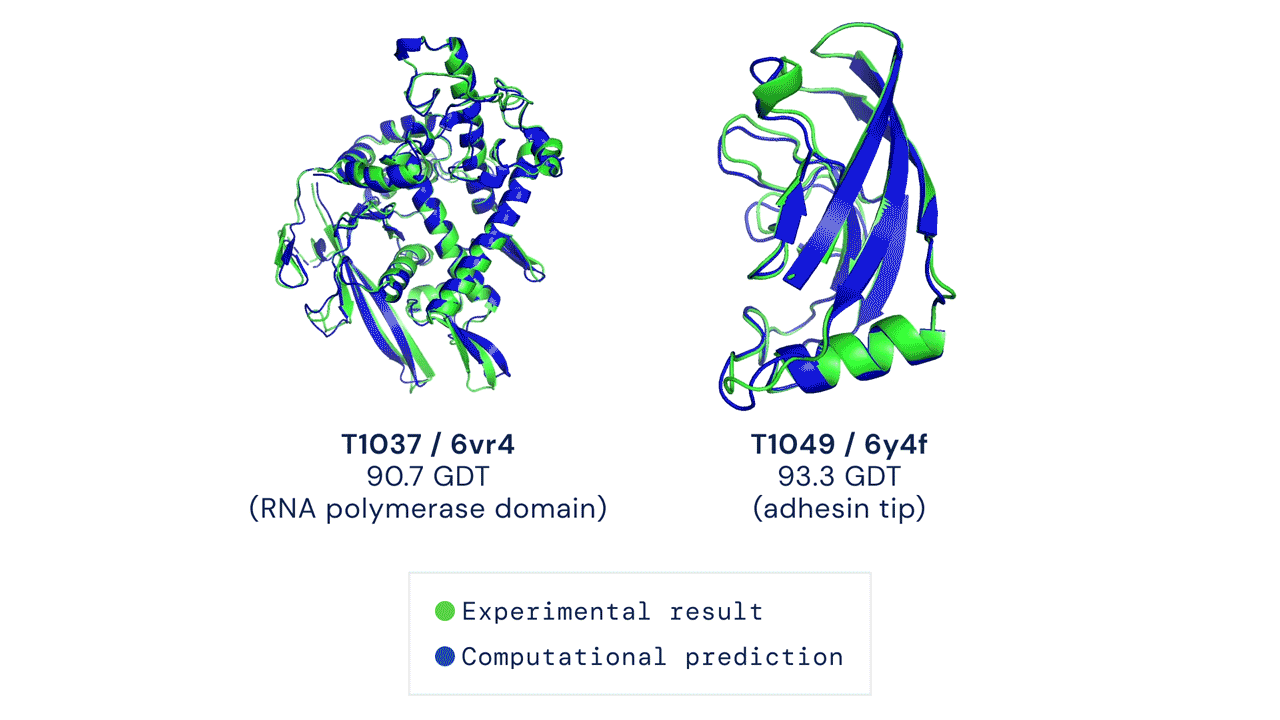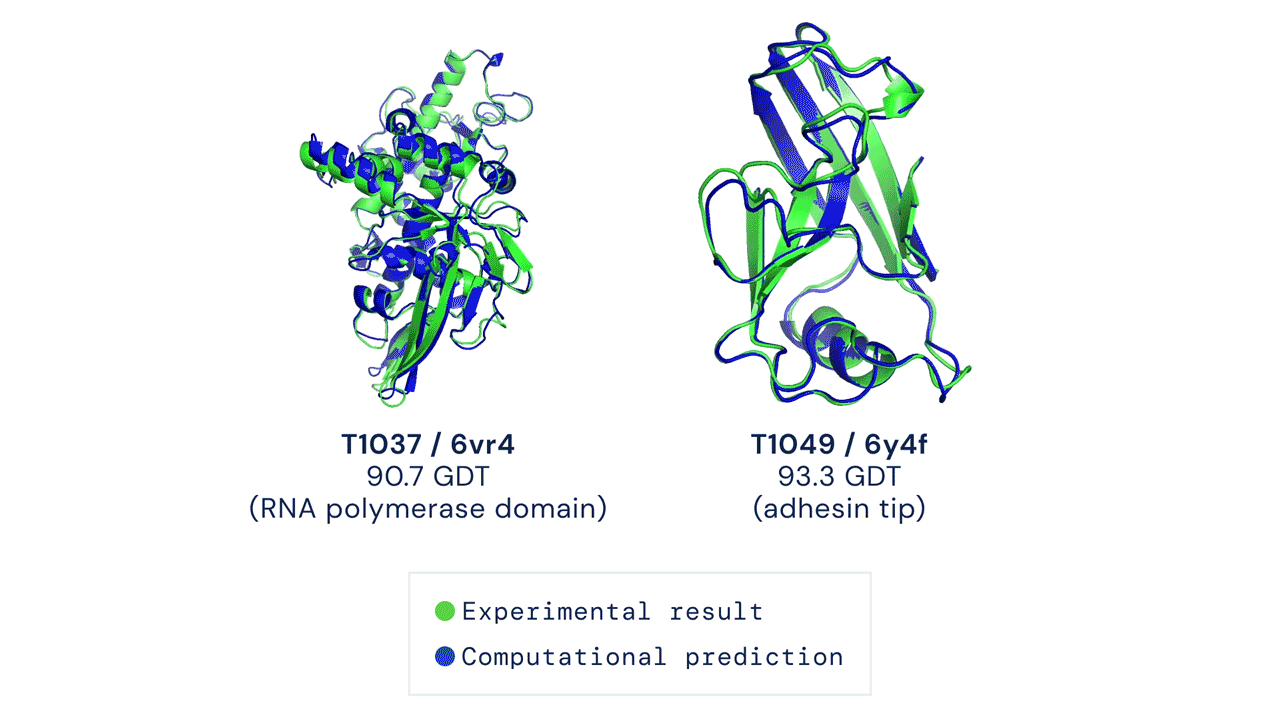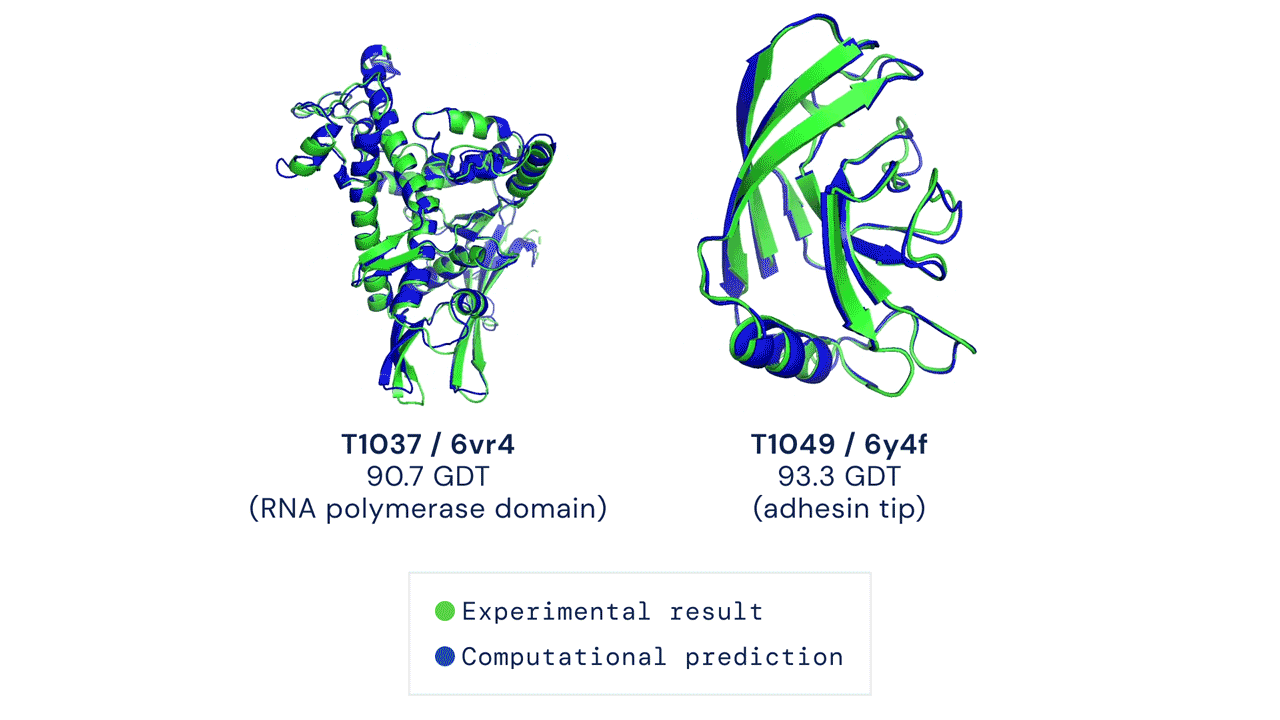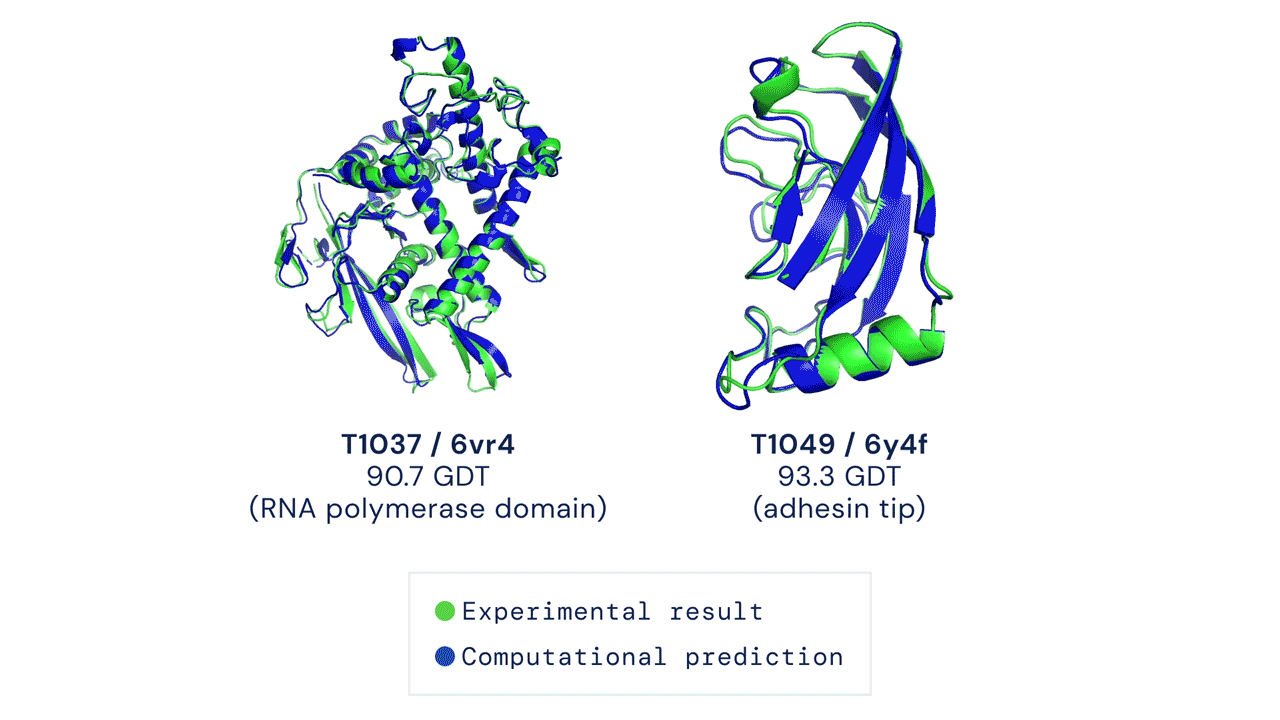
De vooruitgang door de jaren heen is te zien in de volgende grafiek. De y-as moeten we opvatten als de mate van perfectie waarin de vorm van het hele eiwit goed wordt voorspeld.
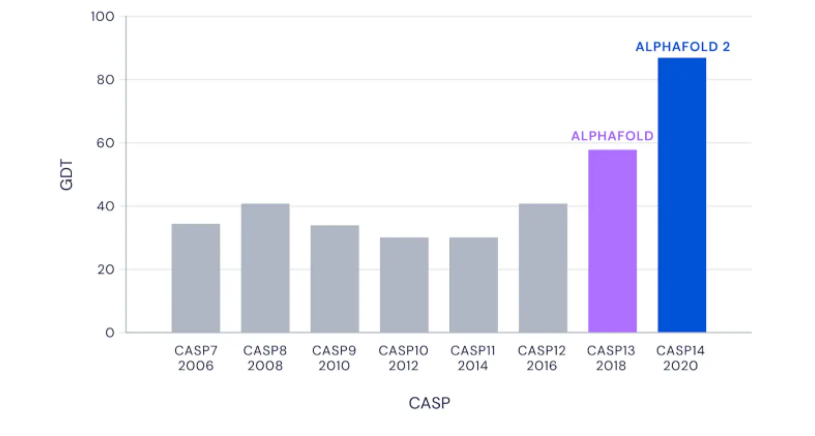
Duidelijk wordt dat er jarenlang maar een langzame vooruitgang was, totdat DeepMind zich ermee begon te bemoeien met zijn software; eerst AlphaFold en nu AlphaFold2.
Revolutie
Deze doorbraak heeft het in zich om een revolutie te ontketenen in de biowetenschappen, zeggen experts. ‘Zelfs kleine veranderingen in deze cruciale moleculen kunnen rampzalige gevolgen hebben voor onze gezondheid’, zegt John Moult, voorzitter van de jury van de CASP-wedstrijd, tegen de BBC. ‘Een van de meest efficiënte manieren om ziekten te begrijpen en nieuwe behandelingen te vinden is dus het bestuderen van de betrokken eiwitten.’
Dure apparatuur
In het menselijk lichaam bestaan er tienduizenden verschillende eiwitten, en vele miljarden in andere soorten, waaronder bacteriën en virussen. Maar voor het uitpuzzelen van de vorm van slechts één eiwit is nu nog dure apparatuur in een laboratorium nodig, en dit kan jaren duren. De software van DeepMind kan dezelfde resultaten boeken door een paar uur te rekenen (op een stuk of honderd speciale processoren), een tijdsduur die volgens sommigen nog verder omlaag kan.
Nieuwe geneesmiddelen
Wat dan gloort aan de horizon is het versnellen van de ontwikkeling van nieuwe geneesmiddelen, nu nog een tergend langzaam proces. Daarnaast kan de nieuwe rekentechniek helpen om bestaande geneesmiddelen te bestuderen en wat die kunnen betekenen voor nieuwe virussen.
 Neem nu het coronavirus. Sinds dat virus zich aandiende zijn wetenschappers al bezig te onderzoeken hoe het spike-eiwit (de stekels op het bolletje, zie de illustratie hiernaast) een wisselwerking aangaat met de receptoren in menselijke cellen. Dit zijn de punten waarop virussen zich kunnen hechten. Als je dit proces kunt verstoren, is dat dus een manier om het coronavirus dwars te zitten.
Neem nu het coronavirus. Sinds dat virus zich aandiende zijn wetenschappers al bezig te onderzoeken hoe het spike-eiwit (de stekels op het bolletje, zie de illustratie hiernaast) een wisselwerking aangaat met de receptoren in menselijke cellen. Dit zijn de punten waarop virussen zich kunnen hechten. Als je dit proces kunt verstoren, is dat dus een manier om het coronavirus dwars te zitten.
DeepMind zou zijn software openbaar moeten maken
Ook bij kanker kan geavanceerd rekenwerk helpen nieuwe geneesmiddelen te ontwikkelen. Bonvin: ‘Sommige vormen van kanker worden veroorzaakt door maar één enkel aminozuur dat verkeerd is in een heel eiwit. Pas als we precies weten welk, dan kunnen we gaan zoeken naar een oplossing, een medicijn dat dit probleem oplost.’
Vrijgeven
Maar voordat de medische wetenschap echt de vruchten kan plukken van het werk van DeepMind, zal het bedrijf eerst zijn software openbaar moeten maken, meent de Utrechtse hoogleraar Bonvin. ‘Als je wilt dat wetenschappers van universiteiten hier nuttig mee aan de slag gaan, dan zal DeepMind de software moeten vrijgeven. Pas dan gaan we echt snel vooruitgang boeken.’
Alpha GO
Het vouwen van eiwitten is niet het eerste schijnbaar onoplosbare probleem waarin de computeringenieurs van DeepMind hun tanden zetten. Het bedrijf zet grote stappen op het gebied van AI en komt eens in de zoveel tijd in het nieuws. Bijvoorbeeld in 2017 toen een AI van DeepMind liet zien beter te zijn in het complexe bordspel GO dan de beste menselijke speler aller tijden.
Daarvan kon je je nog afvragen wat het nut voor de maatschappij was, maar sinds gisteren is duidelijk dat DeepMind (samen met enkele andere bedrijven) de gezondheidszorg misschien wel op zijn kop gaat zetten.
Verder lezen bij Nature, de BBC en The New York Times ($).
Beeldmateriaal DeepMind







