Speciaal implantaat behandelt botinfectie
Ierse onderzoekers hebben een nieuwe manier bedacht om lastige botinfecties te behandelen. Ze ontwierpen een nieuw materiaal, dat artsen als implantaat in het ontstoken bot aan kunnen brengen. Koperdeeltjes in het materiaal doden bacteriën, wat behandeling met antibiotica overbodig maakt.
Een botinfectie wordt soms veroorzaakt door bacteriën die afkomstig zijn van elders in het lichaam; soms ontstaat de ontsteking door een open wond of bij een operatie. De standaardbehandeling van botinfectie is een wekenlange antibioticakuur. Er wordt gezocht naar alternatieven, omdat te veel antibiotica kunnen leiden tot resistentie. Daarnaast is de behandeling in 30 % van de gevallen niet effectief.

Onderzoekers van het Royal College of Surgeons in Ireland (RCSI) hebben nu een nieuwe techniek bedacht om botinfecties aan te pakken. Ze schrijven erover in een artikel in het wetenschappelijke tijdschrift Biomaterials.
Bacteriën doden
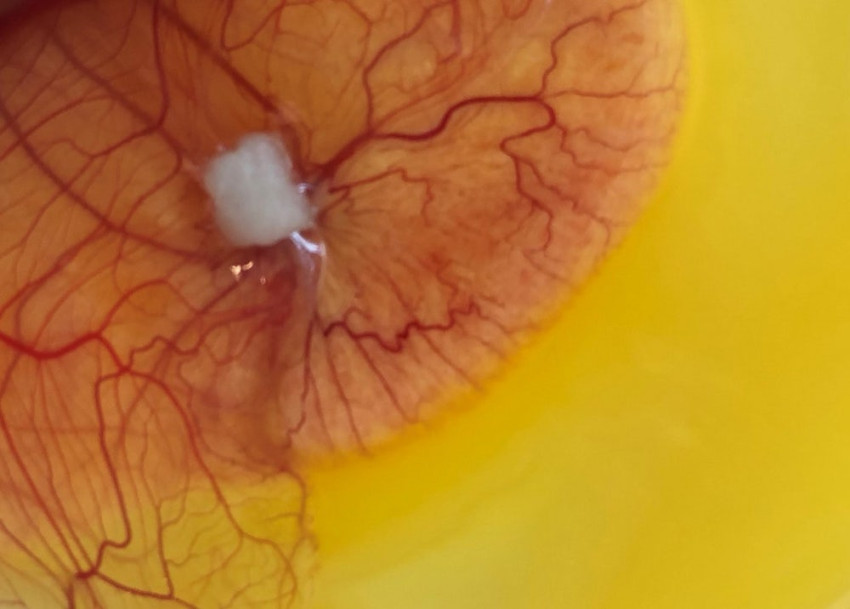
De Ieren maakten een schijfvormig implantaat (diameter 10 millimeter, dikte 5 millimeter) dat op de plek van de infectie komt te zitten. Daar doet het kleine stukje materiaal drie dingen: het doodt bacteriën, het stimuleert de aanmaak van nieuwe bloedvaten en laat nieuw bot groeien.
Het implantaat is gemaakt van een combinatie van collageen (een lichaamseigen stof) en bioactief glas, dat veel gebruikt wordt om beschadigd bot te repareren. Het materiaal is heel poreus, zodat nieuwe bloedvaatjes door het materiaal heen kunnen groeien. Ook zijn de poriën aantrekkelijk voor botcellen om zich in te nestelen. Doen voldoende losse botcellen dat, dan groeit het bot aan elkaar en is er sprake van nieuw botweefsel.
Koperdeeltjes
Het derde ingrediënt van het implantaat zijn koperdeeltjes. Die maken bacteriën dood, via verschillende mechanismen. Bij experimenten met het implantaat in het lab ging tot 66 % van populaties Staphylococcus aureus dood. Tegelijk groeide het nieuwe bot ruim drie keer sneller aan dan in eerdere experimenten.
Behandeling
Het implantaat is inmiddels getest op proefdieren. Voordat het kan worden gebruik in mensen, is nog meer onderzoek nodig. ‘We hopen - en denken - dat dit uiteindelijk kan leiden tot een commercieel verkrijgbare en eenvoudig uitvoerbare behandeling’, zegt promovendus Emily Ryan van RCSI, eerste auteur van de studie in een persbericht.
Haar begeleider denkt ook dat dit pas het begin is. ‘We gaan ons platform aanpassen, zodat je er ook andere antibacteriële stoffen in kunt stoppen. Misschien kunnen we ook wel andere soorten infecties op deze manier bestrijden’, zegt Fergal O'Brien, hoogleraar Bioengineering & Regenerative Medicine.
Openingsbeeld: Het implantaat is getest in het embryo van een kip, om te kijken of het niet zou worden afgestoten. Foto: Emily Ryan / RCSI






