
Kunstmatige alternatieven voor vitale organen
Het functioneren van menselijke organen maakt het verschil tussen leven en dood. Medische technologen werken hard aan kunstmatige alternatieven. Daarbij boeken ze vooruitgang, al gaat dat langzaam.
Patiënten met complexe aandoeningen zijn soms geholpen met een orgaantransplantatie. Ondanks de invoering van de donorwet, waardoor sinds 2020 in principe iedere volwassene na overlijden zijn organen voor transplantatie beschikbaar stelt, bestaan er echter nog altijd grote tekorten, met soms jarenlange wachttijden.
De behoefte aan nieuwe technologie om de functie van falende organen over te nemen is daarom groot. Neem de alvleesklier of pancreas, die de bloedsuikerspiegel reguleert. Medisch technologen werken aan apparaatjes om diabetespatiënten te helpen. Zo’n apparaat meet het glucosepeil in het bloed en als dat te hoog of te laag is geeft het respectievelijk insuline of glucagon af.
‘Dit werkt zonder biologisch materiaal’, zegt Dimitrios Stamatialis, hoogleraar (bio)artificial organs en leider van de groep Advanced organs bioengineering and therapeutics aan de Universiteit Twente. ‘Hier bestaan al verschillende versies van. Eén ervan werkt met een sensorpleister die metingen aan het bloed doorgeeft aan een kastje dat de gebruiker draagt en dat synthetische insuline afgeeft.’
De volgende stap is een biokunstmatige pancreas. Daarin zijn het levende menselijke pancreascellen die het glucosegehalte meten en de aanmaak van insuline of glucagon stimuleren, net zoals ze dat in een gezond lichaam doen.
Hier ligt de uitdaging in de afweerreactie die niet-lichaamseigen cellen kunnen opwekken. Om een patiënt te helpen met een biokunstmatige pancreas moet die cellen bevatten van organen die niet geschikt zijn voor transplantatie of cellen die in het lab zijn geproduceerd uit bijvoorbeeld stamcellen.
Het is niet zo dat het recept dat werkt voor de alvleesklier ook op andere organen kan worden toegepast. Het onderzoek naar kunstmatige varianten is bij sommige organen al behoorlijk gevorderd, maar er zijn ook organen die nog lang niet kunnen worden vervangen door een kunstmatige evenknie, zoals de lever. Wel kan het onderzoek naar het ene kunstorgaan profiteren van de kennis die bij een ander orgaan is opgedaan.
Op de komende pagina’s lichten we er enkele organen uit. Hoe ver staat het met de kunstnier? Is er al een lab-alternatief voor de baarmoeder? Hoe ver staat de ontwikkeling van het kunsthart? Of we ooit zonder donororganen kunnen, blijft intussen maar zeer de vraag. Bioingenieurs werken hard aan compleet ge-engineerde systemen, maar snel gaat dat niet. Stamatialis houdt hoop. ‘We boeken vooruitgang, één orgaan per keer.’

Dit zijn, kort samengevat, de kunstorganen die De Ingenieur brengt in het openingsverhaal van de editie mei 2023:
Kunstnier in een koffer
Wie lijdt aan een nierfalen of nierziekte moet drie keer per week naar het ziekenhuis om bloed te laten schoonspoelen door een dialyseapparaat. Een oplossing is een transplantatie, maar daarvoor zijn er te weinig donornieren. Een draagbare ‘kunstnier’ zou verlichting geven.
Couveuse 2.0
Om het zeer prille leven in een meer natuurlijke omgeving nog even verder te laten groeien, werken onderzoekers samen met specialisten en de industrie aan de TU Eindhoven aan een kunstbaarmoeder en aan de Universiteit Twente aan een kunstplacenta.
Bij openingsbeeld: een hulpstuk ontwikkeld door de TU/e om de vroeggeborene in vloeistof van de moeder naar de kunstbaarmoeder over te brengen. Foto Bart van Overbeeke
Twee kamers en een pomp
Hoewel het volledige kunsthart steeds beter wordt, is een donorhart nog altijd superieur.
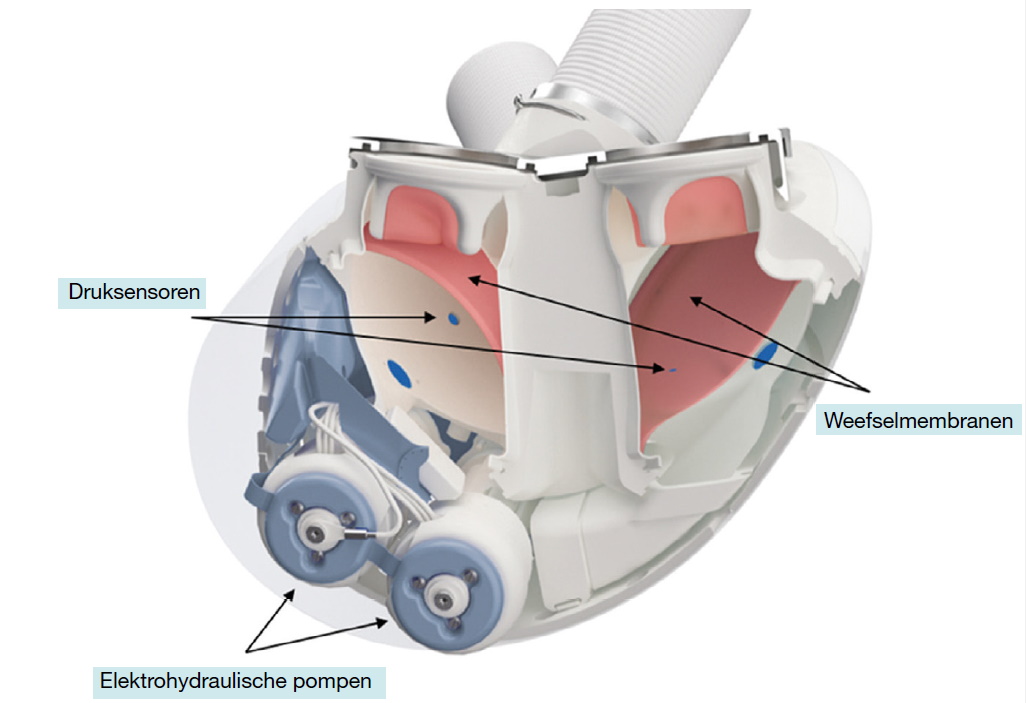
door weefselmembraan. Micropompen sturen het hart aan. Illustratie: Schroder et al., Ann. Thorac. Surg. Short Reports (2023) 1:185-187






